Die Hydra und das Geheimnis des (fast) ewigen Lebens
Die Hydra und das Geheimnis des (fast) ewigen Lebens
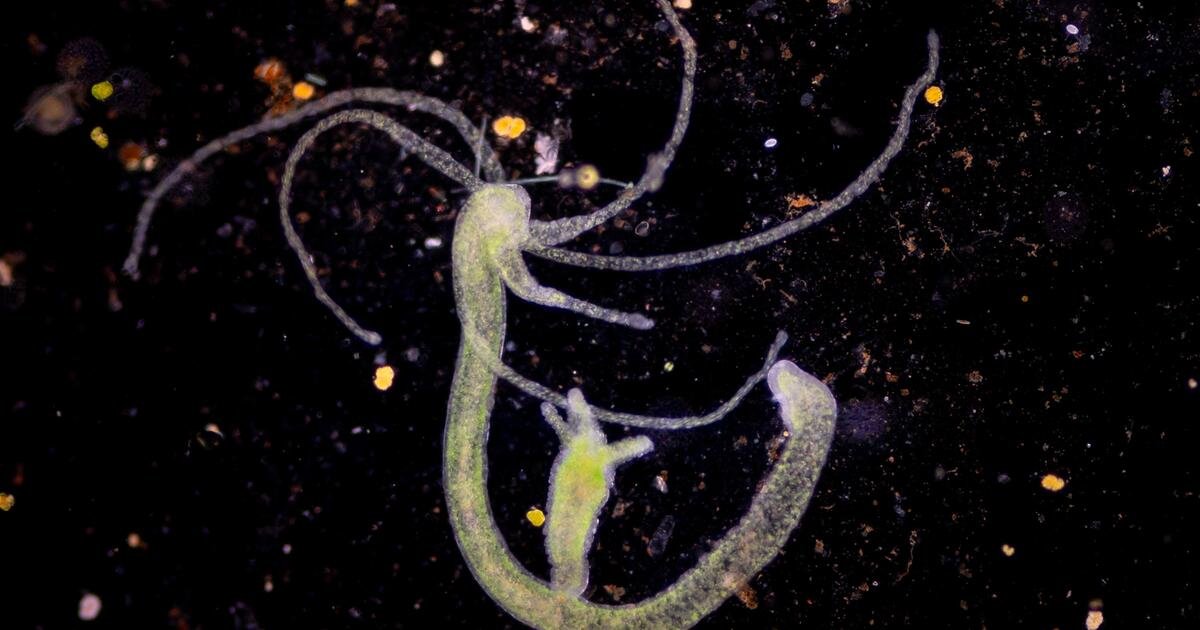
Aktualisiert am 14.05.2026, 22:25 Uhr Der maximal drei Zentimeter große Hydra-Süßwasserpolyp, der in Teichen und Seen lebt, kann laut Forschenden bis zu 1.400 Jahre alt werden und ist damit für die Forschung besonders interessant. © Getty Images/Sinhyu Lesedauer:5 Min. Von Tim FrischeUnscheinbar, aber fast unsterblich: Die Hydra, ein winziger Süßwasserpolyp, kann dank ständig erneuerbarer Stammzellen theoretisch über 1.000 Jahre alt werden. Für die Forschung liefert das Nesseltier faszinierende Einblicke in das Altern, denn seine Gene und sein Mikrobiom zeigen Mechanismen, die auch für den Menschen von Bedeutung sind.
Sie ist winzig klein, doch für die Wissenschaft von großer Bedeutung: Die Hydra, ein maximal drei Zentimeter großer Süßwasserpolyp, der in Teichen und Seen lebt, ist für eine außergewöhnliche Fähigkeit bekannt – sie kann sich ständig erneuern. Die zahlreichen Stammzellen des Nesseltiers teilen sich dauerhaft und ersetzen alte oder beschädigte Zellen, sodass kaum Alterungsprozesse auftreten. Aufgrund dieser besonderen Regenerationsfähigkeit wird sie häufig auch als "unsterbliches" Tier bezeichnet.
Interview Longevity Forscher benennt den "am meisten übersehenen Faktor für ein langes Leben" 11. März 2026 von Sophie BierentDer Zell- und Entwicklungsbiologe Thomas Bosch, der seit Jahrzehnten zur Hydra forscht, betont im Gespräch mit unserer Redaktion jedoch, dass diese Bezeichnung irreführend sei. "Es gibt keine unsterblichen Tiere auf dieser Erde", sagt er. Dies gelte auch für die Hydra, die laut Forschenden bis zu 1.400 Jahre alt werden kann. Vielmehr habe die Evolution bei manchen Organismen besondere Strategien hervorgebracht. "Die sogenannte Unsterblichkeit der Hydra beruht vor allem darauf, dass sie sich über lange Zeiträume ungeschlechtlich durch Knospung fortpflanzen kann." Dabei entstehen in regelmäßigen Abständen neue Polypen aus Stammzellen des Elterntiers. "Alle dreieinhalb Tage bildet das Tier eine neue Knospe. Dafür braucht es Stammzellen, die sich ständig erneuern."
Forschende wollen Altern des Menschen besser verstehen
Solche Organismen mit ungewöhnlichen Lebensspannen sind für die Forschung besonders interessant. "Es gibt viele Tiere, die sehr langsam altern. Und die sind natürlich für die Forschung sehr spannend, weil wir herausfinden können: Warum werden sie semi-unsterblich?", erklärt Bosch. Gleichzeitig gebe es auch das andere Extrem: Tiere, die sehr kurz leben und ihren gesamten Lebenszyklus in kürzester Zeit durchlaufen. Ein prominentes Beispiel aus der Altersforschung ist der Killifisch. "Dieser lebt nur etwa drei Monate und macht in dieser Zeit den ganzen Job für sein Leben – jung sein, sich fortpflanzen und altern", sagt Bosch. Solche Arten mit extrem unterschiedlichen Lebensdauern dienen der Forschung als Modellorganismen, um die biologischen Mechanismen des Alterns zu entschlüsseln.
Die Erkenntnisse daraus sollen langfristig helfen, auch das Altern des Menschen besser zu verstehen. "Wir arbeiten an Modellorganismen, um Konzepte herauszufinden, die auch für den Menschen von Bedeutung sind", sagt Bosch. Im Kern beruhe Altern auf zwei großen Einflussfaktoren: Genetik und Umwelt. Wie stark beide jeweils wirken, ist Gegenstand wissenschaftlicher Diskussion. Bosch schreibt der Genetik rund 20 bis 30 Prozent zu, der Umwelt etwa 70 Prozent.
Einstellung zum Altern beeinflusst die Lebensdauer
Aktualisiert am 09.03.2026, 11:25 Uhr Eine neue Studie stellt alles auf den Kopf, was wir über das Altern zu wissen glaubten: Wer dem Altern positiv gegenüber steht, hat bessere Chancen auf ein längeres Leben. Die eigene Haltung könnte damit entscheidend für Gesundheit und Lebensdauer sein.FOXO-Gen führt zu längerer Lebenserwartung
Auf genetischer Ebene haben Forschende bereits in den 1990er-Jahren mehrere sogenannte Langlebigkeitsgene identifiziert. Besonders bekannt ist das FOXO-Gen (Forkhead-Box-O-Gen). Studien zeigen, dass bestimmte Varianten dieses Gens bei Menschen, die außergewöhnlich alt werden, häufiger vorkommen. Solche Untersuchungen stammen unter anderem aus Regionen, in denen besonders viele Hundertjährige leben – den sogenannten "Blue Zones". Dazu gehören etwa Okinawa in Japan oder Teile Sardiniens in Italien.
Interessanterweise spielt das FOXO-Gen auch bei der Hydra eine zentrale Rolle. In Boschs Labor wurden die Stammzellen des Polypen mit modernen molekularbiologischen Methoden untersucht, und die Forschenden stießen auf mehrere Transkriptionsfaktoren – Gene, die als molekulare Schalter andere Gene steuern. "Einer dieser Transkriptionsfaktoren ist FOXO", erklärt Bosch.
Ausgeschaltetes FOXO-Gen führt zu Alterungsprozessen bei der Hydra
Der Vorteil der Hydra liegt darin, dass sich solche Gene experimentell untersuchen lassen. "Beim Menschen lassen sich nur Korrelationen beobachten: Man vergleicht ältere und jüngere Personen und stellt fest, dass ältere Menschen mehr FOXO besitzen. Daraus lässt sich aber nicht schließen, dass FOXO direkt das Altern steuert", sagt Bosch. In der Hydra hingegen ließ sich FOXO gezielt ausschalten. "Plötzlich begannen die Tiere zu altern: Sie vermehrten sich langsamer und die Stammzellen erneuerten sich nicht mehr richtig." Damit konnte kausal gezeigt werden, dass FOXO eine zentrale Rolle bei Alterungsprozessen spielt – ein Nachweis, der am Menschen experimentell nicht möglich ist.
Doch Gene sind nur ein Teil der Geschichte, die Umwelt ein weiterer. Und zu dieser gehört das Mikrobiom – also die Gesamtheit der Bakterien, die im und auf unserem Körper leben. Diese Mikroorganismen besiedeln den Darm, die Haut und viele andere Bereiche des Körpers und verändern sich im Laufe des Lebens. "Vom Neugeborenen über den Erwachsenen bis zum alten Menschen verändert sich das Mikrobiom", erklärt Bosch.
Hohe LDL-Werte Sind Eier, Butter und Käse wirklich schuld am hohen Cholesterinspiegel? 10. März 2026Der Killifisch als spannendes Gegenbeispiel
Wie stark solche Mikroben Alterungsprozesse beeinflussen können, zeigen Experimente mit anderen Modellorganismen. Der Altersforscher Dario Valenzano konnte beispielsweise in einer 2017 veröffentlichten Studie nachweisen, dass sich alte Killifische verjüngen lassen, wenn man ihnen das Darmmikrobiom junger Tiere überträgt. Das zeige sich unter anderem an ihrer Beweglichkeit, ihrem Verhalten, ihrer kognitiven Leistungsfähigkeit sowie an verschiedenen physiologischen Parametern. Ähnliche Experimente wurden später auch bei Mäusen durchgeführt – mit vergleichbaren Ergebnissen.
Auch bei der Hydra scheint es eine enge Verbindung zwischen Genetik, Mikrobiom und Alterung zu geben. Das FOXO-Gen beeinflusst über das Immunsystem auch die Zusammensetzung der Bakteriengemeinschaft des Polypen. "Diese Tiere haben ein erstaunlich stabiles Mikrobiom, das sich über ihr ganzes Leben hinweg nicht verändert", erklärt Bosch. Wird das FOXO-Gen ausgeschaltet, verändert sich auch diese bakterielle Gemeinschaft deutlich. "Wir vermuten, dass dieses veränderte Mikrobiom kausal an den Alterungsprozessen beteiligt ist."
Parabiose führt zu Verjüngungseffekten
Ein weiterer Hinweis auf die Bedeutung solcher Faktoren ergibt sich aus klassischen Experimenten der Altersforschung, insbesondere aus Parabiose-Experimenten. Dabei werden zwei Versuchstiere chirurgisch so verbunden, dass sie einen gemeinsamen Blutkreislauf teilen. "Wenn man ein junges Tier mit einem alten zusammennäht, wird das alte Tier tatsächlich jünger", sagt Bosch. Der einzige Austausch zwischen beiden Organismen sei dabei das Blut.
Warum genau das so ist, ist allerdings noch nicht vollständig geklärt. Ein möglicher Hinweis liegt darin, dass ein beträchtlicher Teil der kleinen Moleküle im Blut von Mikroorganismen stammt. "Heute wissen wir, dass etwa 20 bis 30 Prozent der Stoffwechselprodukte im Blut von Bakterien produziert werden", sagt Bosch. Ob diese mikrobiellen Moleküle tatsächlich für die beobachteten Verjüngungseffekte verantwortlich sind oder ob andere Faktoren eine Rolle spielen, wird derzeit intensiv untersucht.
Der Traum vom ewigen Leben bleibt ein Traum
Und was bedeuten diese Forschungen für den Menschen? Rückt der "Jungbrunnen" – oder gar eine Unsterblichkeit – in greifbare Nähe? Bosch schiebt dieser Vorstellung einen Riegel vor. "Das maximale Lebensalter des Menschen ist genetisch weitgehend festgelegt", sagt er. Wahrscheinlich werde kein Mensch deutlich älter als etwa 120 Jahre. Ziel sei es ohnehin nicht, das Leben unbegrenzt zu verlängern. "Uns geht es in der Altersforschung darum, ein gesundes Altern zu ermöglichen."
Empfehlungen der Redaktion
- Wie eine Hummel acht Tage unter Wasser überlebt
- Schwer wie ein Elefant: Dieses Organ des Blauwals ist das schwerste im Tierreich
- Wie ein behinderter Papagei alle Rivalen in die Flucht schlägt
Genau hier könnten Erkenntnisse aus der Forschung an Hydra, Killifisch und anderen Modellorganismen langfristig helfen. "Diese Tiere zeigen uns, welche Mechanismen die Natur beim Altern – und beim Nichtaltern – einsetzt", erklärt Bosch. "Sie liefern grundlegende Konzepte, die uns helfen können, zu verstehen, wie wir das Altern des Menschen besser beeinflussen können."
Über den Gesprächspartner
- Prof. Dr. Thomas Bosch ist Zell- und Entwicklungsbiologe und Professor an der Christian-Albrechts-Universität zu Kiel. Seit vielen Jahren erforscht er Modellorganismen wie die Hydra, um grundlegende Mechanismen von Entwicklung, Alterung, Immunität und der Wechselwirkung zwischen Organismen und ihrem Mikrobiom zu verstehen. Für seine Arbeiten zur Evolutionsbiologie und zur Bedeutung von Mikroorganismen für Gesundheit und Altern wurde er mehrfach ausgezeichnet.
